Зарегистрируйтесь, чтобы делать покупки, отслеживать заказы и пользоваться персональными скидками и баллами.
Зарегистрируйтесь, чтобы делать покупки, отслеживать заказы и пользоваться персональными скидками и баллами.

Очень часто в фильмах хлороформ показывают, как успокоительное, которое действует за секунды и является очень эффективным, человека усыпляют мгновенно. В действительности дела обстоят иначе, а сам хлороформ из-за его высокой токсичности в настоящее время очень ограничен в применении в промышленности.
Очень часто в фильмах хлороформ показывают, как успокоительное, которое действует за секунды и является очень эффективным, человека усыпляют мгновенно. В действительности дела обстоят иначе, а сам хлороформ из-за его высокой токсичности в настоящее время очень ограничен в применении в промышленности.
Определение
Хлороформ, трихлорметан (лат . chloroform ) — органическое химическое соединение из группы галогеналканов — хлорпроизводное метана. Это бесцветная и малореактивная жидкость. Хлороформ в основном используется в качестве растворителя, например, при анализе окружающей среды или хроматографии (метод разделения химических соединений). Из-за высокой токсичности его заменяют хлористым метиленом. Длительное вдыхание может привести к интоксикации, анестезии и седативному эффекту.
Важно! Хлороформ, или трихлорметан, был открыт в 1831 году опытным путем как растворитель для каучука Самуэлем Гутри. Его точную формулу в 1834 году установил химик Дюма, который и дал веществу название «хлороформ» (от лат. acidum formicum – «муравьиная кислота» – из-за образования ее из хлороформа.
Характеристики
Хлороформ в комнатных условиях представляет собой густую бесцветную жидкость со сладковатым запахом. Он имеет острый вкус и вызывает жжение во рту. Он негорюч и мало вступает в реакцию с другими химическими веществами. Пары хлороформа под действием пламени разлагаются, в результате чего образуются, в том числе, хлор, хлористый водород и фосген (сильно ядовитый и удушающий газ). Реакция разложения также протекает при воздействии солнечного света, но в меньшей степени. В результате хлороформ очень часто загрязняется вышеуказанными веществами разложения. Купить хлороформ можно в нашем интернет-магазине.
|
Хлороформ |
Свойства |
|
Наименование |
Трихлорметан, метилтрихлорид, формилтрихлорид |
|
Химическая формула хлороформа |
CHCl₃ |
|
Молярная масса |
119,38 г/моль |
|
Плотность |
1,4788 г/см³ |
|
Растворимость воды |
8,0 г/кг (25°С), 7,9 г/кг (59°С) |
|
Температура плавления |
−63,47°С |
|
Точка кипения |
61,2°С |
|
Критическая точка |
262,9°С |
Современное применение и использование хлороформа
Сегодня хлороформ чаще всего встречается в растворителях красок и масел, а также в препаратах, облегчающих удаление жира, а также в химчистках. Продукты, содержащие это вещество, всегда содержат информацию о нем, а на их упаковке можно прочитать предупреждение о негативных последствиях отравления хлороформом. Хлороформ также является источником радикалов (атомов или молекул, содержащих неспаренные электроны) в органическом синтезе.
Производство
Хлороформ получают в промышленности путем нагревания хлора с метаном или хлорметаном до 400–500 °С. При этой температуре происходит ступенчатое радикальное замещение до четыреххлористого углерода:
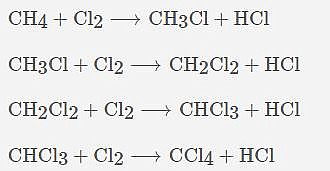
Применение хлороформа в медицине и действие на человека
В прошлом медицина также использовала особые свойства хлороформа. Чистый хлороформ (Chloroformium anaestheticus ) использовался с 1847 года для введения пациентов в состояние глубокой анестезии. Не менее популярными средствами с аналогичным действием были тогда диэтиловый эфир и закись азота. Анестезиологи применяли «хлороформ» с концентрацией 1% во вдыхаемом воздухе. Стоит отметить, что врачи буквально играли со смертью, ведь несколько более высокая концентрация хлороформа, достигающая 1,3-1,5%, вызывает у человека паралич дыхательного центра.
Но почему же было решено использовать хлороформ, если грань между анестезирующим средством и убивающей концентрацией была так тонка? В первую очередь это было связано с тем, что хлороформный наркоз проходил спокойнее и быстрее, чем в случае с эфиром (к сожалению, для пробуждения больного требовалось больше времени). В межвоенный период от хлороформного наркоза постепенно отказались в пользу более безопасных мер.
В настоящее время хлороформ все еще используется в медицине, в частности в дерматологии и ревматологии, хотя это очень редкие случаи. Его использование ограничено рецептурными препаратами для местного применения.
Где встречается хлороформ
Хлороформ встречается в природе. Подсчитано, что каждый год в атмосферу выбрасывается около 660 тонн хлороформа, 90% которого поступает из природных источников. Хлороформ получают, в том числе, макроводорослями и, скорее всего, грибами, которые выделяют это соединение прямо в грунт. Хлороформ легко испаряется с поверхности почвы и воды, что приводит к разложению в воздухе с образованием таких соединений, как фосген, дихлорметан, ацилхлориды, монооксид углерода и хлористый водород. Период полураспада хлороформа составляет от 55 до 620 дней и его биоразложение в воде и почве происходит очень медленно. Хлороформ практически не накапливается в организме гидробионтов.
Вред хлороформа

Хлороформ очень вреден для здоровья. Раздражает глаза и кожу. Его длительное вдыхание или потребление в высоких концентрациях может привести к нарушениям или остановке сердца и дыхания. В более низкой концентрации вызывает чувство сонливости и оказывает депрессивное действие (этот эффект сохраняется длительное время). Кроме того, хлороформ повреждает почки и печень. Многие данные и классификация хлороформа указывают на то, что он канцерогенен.
Порядок действий при отравлении
Первая помощь при отравлении хлороформом ограничивается вызовом скорой помощи и принятием мер по защите больного. Важно транспортировать пациента подальше от источника хлороформа, если это возможно, снять всю одежду, на которую было пролито химическое вещество, и вымыть кожу водой с мылом. Важно начать с информирования соответствующих служб, опираясь на их оценку ситуации и следуя их указаниям. Хлороформ больше не классифицируется как лекарственное вещество, особенно доступное в аптеках, будь то по рецепту или без рецепта. Его можно приобрести в качестве химического реагента или растворителя, и только такое использование соответствует предполагаемому использованию этих продуктов.
