Зарегистрируйтесь, чтобы делать покупки, отслеживать заказы и пользоваться персональными скидками и баллами.
Зарегистрируйтесь, чтобы делать покупки, отслеживать заказы и пользоваться персональными скидками и баллами.

Амины представляют собой органические химические соединения, имеющие аминогруппу (-NH2,-NHR,-NR'R). Это производные аммиака - атомы водорода заменены углеводородными группами.
Амины представляют собой органические химические соединения, имеющие аминогруппу (-NH2,-NHR,-NR'R). Это производные аммиака - атомы водорода заменены углеводородными группами. В зависимости от того, сколько органических заместителей присоединено к атому азота, различают три типа аминов: I-, II- и III-порядка, схематически представленные ниже. Известны также четвертичные аммониевые соединения R 4 N + (катионы и соли).
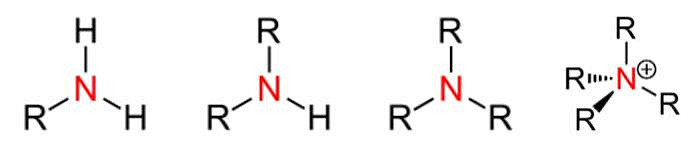
В зависимости от молекулярной массы амины представляют собой газы, например:
- метиламин - CH3-NH2,
- диметиламин (CH3)2NH,
- триметиламин - (CH3)3N
жидкости или твердые вещества (анилин).
Физические свойства
Короткоцепочечные алифатические амины хорошо растворяются в воде и имеют характерный рыбный запах. Подобно спиртам, благодаря наличию сильно электроотрицательного элемента, т. е. азота, молекулы аминов могут образовывать водородные связи, что, по-видимому, снижает их летучесть.
Амины получают алкилированием аммиака галоидными алкилами. Эта реакция представляет собой нуклеофильное замещение, в котором нуклеофильным агентом является аммиак. Амины также являются продуктами восстановления соединений, содержащих азот в степени окисления выше, чем -III, например, нитрозо-, нитро-, азосоединений.
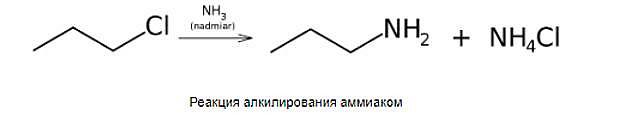
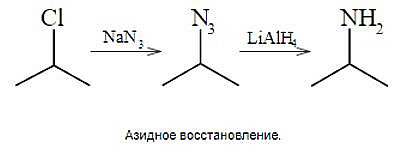
Амины проявляют большую реакционную способность. Это связано с наличием неподеленной пары электронов у атома азота, который обычно является центром протекающих реакций. По этой причине амины обладают основными свойствами. Алифатические амины являются более сильными основаниями, а ароматические - более слабыми, чем аммиак. В реакциях с неорганическими кислотами в зависимости от порядка дают моно-, ди- или триалкиламмониевые соли. Реакции аминов с азотной (III) кислотой важны, так как они используются для определения порядка аминов и для различения алифатических и ароматических аминов:
- в случае первичных алифатических аминов выделение бесцветного газа (азота) будет наблюдаться при температуре ниже 5°C,
- реакция с первичным ароматическим амином также приводит к выделению бесцветного газа (азота), но для этого требуется более высокая температура,
- при наличии в испытуемом образце вторичного амина (ароматического или алифатического) наблюдается желтая маслянистая жидкость,
- реакция с третичными алифатическими аминами не дает видимых эффектов,
- в случае ароматических третичных аминов раствор окрашивается в оранжевый цвет.
В результате реакции аминов с органическими кислотами образуется пептидная связь:
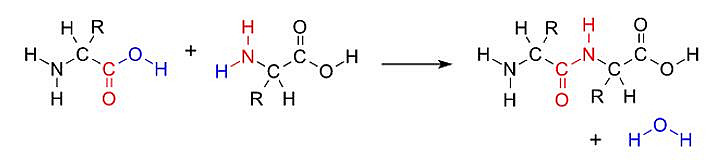
Первичные амины также реагируют с альдегидами и кетонами с образованием альдиминов или кетиминов. Амины обладают слабыми кислотными свойствами, но с сильными основаниями (например, NaOH) они образуют амидные соли. Атом азота, присутствующий в аминах, находится в низшей степени окисления, поэтому они устойчивы к восстановлению. Аминогруппа, обработанная окислителем (например, KMnO4), окисляется до нитрильной группы (-NO2)
R-NH2 → R - NO2
В случае ароматических аминов аминогруппа сильно активирует ароматическое кольцо и направляет следующие заместители в орто- и пара -положения.
Названия первичных аминов строятся с использованием корня «амин» и перечислением углеводородных заместителей в алфавитном порядке. При наличии нескольких аминогрупп на это указывает добавление префикса ди-, три- перед основой «амин». Для вторичных и третичных аминов выбирается наиболее важная углеводородная группа, а названия остальных указываются как заместители с префиксом N, чтобы указать, что они присоединены к остальной части молекулы через атом азота.
Амины широко распространены в природе, где они участвуют в круговороте азота. Они используются в фармацевтической и химической промышленности для производства красок, волокон и поверхностно-активных веществ. Ароматические амины канцерогенны.
Также благодаря своей основности и хорошей растворимости в воде амины находят ряд применений: многие из применяемых сегодня лекарств содержат аминогруппы; амины с более простой структурой также являются строительными блоками для синтеза более сложных соединений. Помимо лекарственных средств можно назвать диазокрасители , полученные из аминов или детергентов, содержащих в своей структуре устойчивые соли аммония, для синтеза которых также необходим амин.
Кроме того, простые амины используются для очистки природного газа от углекислого газа и сероводорода в процессе нефтепереработки.
